Bio-PAT auf dem 6. BioProScale Symposium
Vom 29.03. bis 31.03.2021 fand das 6. BioProScale Symposium das erste Mal virtuell statt. Das Symposium wurde vom Fachgebiet der Bioverfahrenstechnik an der Technischen Universität Berlin, dem Institut für Gärung und Biotechnologie in Berlin (IfGB) als Teil der Versuchs- und Lehranstalt für Brauerei in Berlin (VLB e.V.) und dem Bio-PAT e.V. organisiert. Normalerweise findet das Symposium alle 2 Jahre vor Ort in Berlin statt (siehe Historie). Diese Tradition wurde nun aufgrund der Corona Pandemie gebrochen. Wir danken allen Beitragenden, Teilnehmern und Sponsoren, dass sie dennoch das neue online Format akzeptiert und den Umgang damit nicht gescheut haben.
224 Teilnehmer aus 19 Ländern registrierten sich für das online Event, 46 aufregende Vorträge aus Industrie und Forschung sowie 33 Posterbeiträge wurden präsentiert und 10 Aussteller zeigten ihre Produkte und Dienstleistungen. Folgende Themen standen auf diesem BioProScale Symposium im Fokus: “Industrial scale bioprocessing and scale down, process analytical technologies (PAT), bioprocesses for a circular economy, microfluidic systems, high-throughput bioprocessing and automation, modelling bioprocesses”.
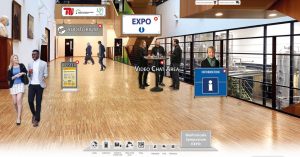
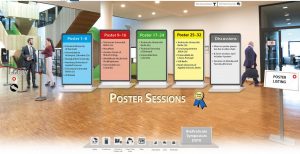
Dank der VLB Berlin wurde eine virtuelle Plattform mit einem Ausstellerbereich, einem Auditorium für Vorträge, einer Poster-Ausstellung, einem Video-Chat-Bereich sowie privaten Chaträumen eingerichtet. Die Plattform war sogar einige Tage vor und nach dem Symposium für registrierte Teilnehmer zugänglich. In dem Video-Chat-Bereich, bereitgestellt von “wonder.me”, trafen sich die Teilnehmer in den Pausen und am Abend, um sich über die Vorträge und Poster zu unterhalten, die Aussteller zu informieren oder sich in verschiedenen Diskussionen und Chats in kleineren Gruppen auszutauschen. Mit Hilfe eines professionellen Aufnahmestudios wurden live Sessions mit der Möglichkeit für interaktive live Diskussionen umgesetzt. Mehr Informationen über die Plattform gibt es hier.
Bio-PAT als Aussteller
Das Netzwerk Bio-PAT war einer der Aussteller, ebenso wie einige seiner Mitglieder, die BlueSens gas sensor GmbH, Celltainer Biosolutions GmbH und Enpresso GmbH. Weitere Mitglieder, wie AdvaTec® Analytics GmbH, Abacus Analytical Systems GmbH, Knick Elektronische Geräte GmbH und Co. KG, Sequip S+E GmbH und SOPAT GmbH stellten ausführlichere Informationen zum Download und als Video-Material auf dem Bio-PAT Stand zur Verfügung.
Über die Integration eines externen Video-Chat-Raums gab es die Möglichkeit für das Netzwerk, sich mit den Mitgliedern und Besuchern des Standes separat zu unterhalten. Es war eine großartige Erfahrung für das Netzwerk, sich auf dieser Plattform auszutauschen und neue Leute und Unternehmen kennen zu lernen.
Auszeichnungen für die besten Vorträge und Poster
Die Organisatoren danken dem MDPI für das Sponsoring der Preise für die besten Vorträge sowie Eppendorf für das Sponsoring der Preise für die besten Poster. Damit wurden die großartigen Arbeiten von jungen Wissenschaftlern gewürdigt.
Wir sind stolz, dass Björn Gutschmann (Fachgebiet Bioverfahrenstechnik an der Technischen Universität Berlin) und Thomas Schiewe (Fachgebiet Physikalische Chemie an der Universität Potsdam / innoFSPEC und PDW Analytics GmbH) den Preis für den besten Vortrag für ihre Präsentation “In-line application of photon density wave spectroscopy as a PAT sensor in high cell-density bioprocesses: Monitoring of E. coli growth and PHA formation in R. eutropha” gewonnen haben. Beide Fachgebiete sowie die PDW Analytics GmbH sind Mitglieder des Bio-PAT Netzwerks. Der 2. Platz ging an Sarah Täuber (Universität Bielefeld) für ihre Präsentation “Dynamic microfluidic single-cell cultivation: Growth of Corynebacterium glutamicum at fluctuating environmental conditions”. Phuong Ho (Forschungszentrum Jülich) erhielt den 3. Preis für seine Präsentation “Reproducing dynamic environment in microfluidic single-cell cultivation based on computational lifeline analysis”. Alle Abstrakte der Gewinner-Vorträge können am Ende des Berichts nachgelesen werden.
Der 1. Preis für das beste Poster ging an Amin Javidanbardan (Universidade de Lisboa) mit dem Postertitel “Rapid and cost-effective fabrication of micro chromatography integrated with microelectrode impedance sensor”, gefolgt von Jian Li (ShanghaiTech University) mit dem Poster “Total in vitro biosynthesis of the nonribosomal macrolactone peptide valinomycin” und Tobias Höing (Mosa Meat) mit “Cultured meat production in a 2D rocking bioreactor”. Mosa Meat ist ein Kooperationspartner des Bio-PAT Mitglieds Celltainer Biosolutions GmbH.
Wir gratulieren allen Gewinnern und wünschen ihnen für ihre zukünftige wissenschaftliche Karriere alles Gute.
Nächstes BioProScale Symposium:
Für Updates treten Sie der BioProScale Gruppe auf LinkedIn bei!
Informationen zu den Organisatoren:
Bioverfahrenstechnik, TU Berlin: https://www.tu.berlin/bioprocess/
VLB Berlin: https://www.vlb-berlin.org/home, LinkedIn, Facebook
Netzwerk Bio-PAT: https://bio-pat.org/, LinkedIn, Facebook, Instagram, Twitter, YouTube
 Wir danken dem Medienpartner q&more für die Bewerbung der Veranstaltung und die Berichterstattung im Nachgang.
Wir danken dem Medienpartner q&more für die Bewerbung der Veranstaltung und die Berichterstattung im Nachgang.
Abstrakte der Gewinner-Vorträge
1. In-line application of photon density wave spectroscopy as a PAT sensor in high cell-density bioprocesses: Monitoring of E. coli growth and PHA formation in R. eutropha
Björn Gutschmann1, Thomas Schiewe1,2,3, Marvin Münzberg2, Peter Neubauer1, Roland Hass3, Sebastian L. Riedel1
1Technische Universität Berlin, Chair of Bioprocess Engineering, Ackerstraße 76, 13355 Berlin, Germany
2innoFSPEC, University of Potsdam, Am Mühlenberg 3, 14476 Potsdam, Germany
3PDW Analytics GmbH, Geiselbergstr. 4, 14476 Potsdam, Germany
Email: riedel@tu-berlin.de
A cost-efficient production process often involves high-cell-density cultivations, which represent challenging surroundings for optical process analytical technologies, due to signal saturation effects and probe fouling. An accurate process monitoring, and control strategy is a key concern for industrial bioprocesses. Addressing this issue, the integration of photon density wave (PDW) spectroscopy into highly turbid multiphase systems enables a novel approach for optical process monitoring. It allows for independent quantification of absorption and scattering properties by measuring the optical coefficients µa and µs’ while being suitable for highest particle concentrations (i.e. >40 vol%) in stirred or flowing systems [1, 2]. This contribution shows the application of a fully autoclavable in-line PDW spectroscopy probe during high-cell-density fed-batch cultivations. Results from Escherichia coli cultivations at 3.7-L scale show excellent correlations between the reduced scattering coefficient µs’ and biomass concentrations up to 76 g L-1. The results will be discussed in comparison to multiple established analytical methods. Additionally, for the first time polyhydroxyalkanoate (PHA) biopolymers formation and growth during cultivations of Ralstonia eutropha, was monitored in-line, simultaneously by separation of absorption and scattering properties using the PDW technology. Results of highcell-density fed-batch cultivations at 6.7-L scale with rapeseed oil [3] and the adaption to waste animal fats will be presented.
1. Bressel, L., Hass, R. and Reich, O. (2013) Particle sizing in highly turbid dispersions by Photon Density Wave spectroscopy. JQRST. 126: 122-129.
2. Hass, R., Munzke, D., Ruiz, S.V., Tippmann, J. and Reich, O. (2015) Optical monitoring of chemical processes in turbid biogenic liquid dispersions by Photon Density Wave spectroscopy. Anal Bioanal Chem. 407: 2791-802.
3. Gutschmann, B., Schiewe, T., Weiske, M.T., Neubauer, P., Hass, R. and Riedel, S.L. (2019) In-Line monitoring of polyhydroxyalkanoate (PHA) production during high-cell-density plant oil cultivations using Photon Density Wave Spectroscopy. Bioengineering. 6: 85.
2. Dynamic microfluidic single-cell cultivation: Growth of Corynebacterium glutamicum at fluctuating environmental conditions
Sarah Täuber1, Luisa Blöbaum1, and Alexander Grünberger1
1Multiscale Bioengineering, Technical Faculty, Bielefeld University, Bielefeld, Germany
Email: sarah.taeuber@uni-bielefeld.de
In large-scale bioreactors, different gradients occur, which lead to a fluctuating supply of oxygen, nutrients and other process parameters that strongly influence the growth and production behaviour of the microbial strains and endanger the success of the scale-up [1]. Scale-down experiments are an established tool to investigate the growth and production related effects of industrial-scale gradients on microorganisms using lab-scale fermenters [2]. However, traditional scale-down approaches are bulk measurements and cannot provide the direct answer to how cells are affected by gradients on a single-cell level [3]. Novel analytical methods need therefore to be developed [4]. In this contribution, we introduce a microfluidic single-cell workflow for the cultivation of microbial cells under dynamic environmental conditions [5]. This system allows oscillation between different environmental input parameters e.g., between pH values or carbon sources. We give an overview into the technology and show how oscillating environmental conditions (here C source and pH value) affect the cellular physiology. In a first study, we cultivated C. glutamicum under oscillating medium conditions (medium rich and buffer) with different oscillation frequencies ranging from hours to seconds intervals [5]. A significant difference within the overall growth behaviour was observed at different oscillations frequencies. Oscillations time between 5 and 15 minutes significantly affect the overall growth rate. At higher oscillations frequencies growth was not impaired significantly. In a second study, we investigated the growth behaviour of C. glutamicum under specific pH oscillations that varied in their pH amplitude and frequency [6]. pH oscillations between discrete pH units decreased the overall growth rate. The decrease was dependent on the stress pH values (e.g., pH=5) and the ratio of pH stress phases to regeneration phase at pH=7. Latest results, hypothesis regarding the observed growth pattern and potential application will be shown. Our results show that the concept of dynamic microfluidic single-cell cultivation has a high potential to investigate cellular physiology at dynamic environmental conditions. This paves the way for an improved understanding of how environmental conditions shape metabolic heterogeneity and thus the cellular response within growth and production upon nutrient and pH gradients within large-scale bioprocesses, often referred as lifeline. In future it is essential to validate the technology with conventional scale-down approaches to further optimize the technology towards novel single-cell scale-down reactors.
1. Takors, R. (2012) Scale-up of microbial processes: impacts, tools and open questions. Journal of biotechnology, 160: 3–9.
2. Delvigne, F. and Noorman, H. (2017) Scale-up/Scale-down of microbial bioprocesses: a modern light on an old issue. Microbial biotechnology, 10: 685–687.
3. Lemoine, A., Maya Martinez-Iturralde, N., Spann, R., Neubauer, P. and Junne, S. (2015) Response of Corynebacterium glutamicum exposed to oscillating cultivation conditions in a two- and a novel three-compartment scale-down bioreactor. Biotechnology and bioengineering, 112: 1220–1231.
4. Grünberger, A., Wiechert, W. and Kohlheyer D. (2014) Single-cell microfluidics: opportunity for bioprocess development. Current opinion in biotechnology, 29: 15-23.
3. Reproducing dynamic environment in microfluidic single-cell cultivation based on computational lifeline analysis
Phuong Ho1, Sarah Täuber2, Alexander Grünberger2, Eric von Lieres1
1Forschungszentrum Jülich, IBG-1: Biotechnology, Wilhelm-Johnen-Str. 1, 52428 Jülich, Germany
2Universität Bielefeld, Multiscale Bioengineering, Universitätsstraße 25, 33615 Bielefeld
Email: p.ho@fz-juelich.de; sarah.taeuber@uni-bielefeld.de
The biotechnological production of valuable substances is typically complicated by the loss of microbial performance upon scale-up [1-3]. This challenge is mainly caused by discrepancies between homogeneous environmental conditions at laboratory scale, where organisms are optimized, and inhomogeneous conditions in large-scale bioreactors, where the production takes place. To improve strain selection and process development, it is thus of major interest to characterize these fluctuating conditions at large scales and investigate their impact on microbial cells. In this contribution, we will demonstrate the high potential of dynamic microfluidic single-cell cultivation combined with computational fluid dynamics (CFD) simulation of large-scale bioreactors. CFD simulations of a 300 L bioreactor were applied to characterize environmental conditions in large-scale bioreactors. So-called lifelines were determined by simulating multiphase turbulent flow and mass transport combined with particle tracing. Glucose availability experienced by the microorganism Corynebacterium glutamicum was traced. Resulting lifelines were discretized into low, medium and high glucose availability regimes. Discretized lifelines were used as feeding profiles of a dynamic microfluidic single-cell cultivation (dMSCC) system to investigate how the fluctuating glucose concentration affects cellular physiology and colony growth rate. The presented approach paves the way for an improved understanding of how the cellular lifelines of large-scale bioreactors influence the cellular response within growth and production. It also provides insights into how to understand the conditions in large-scale bioreactors from the view of a microorganism and the dependence of cell wellbeing on the observed conditions.
1. Oosterhuis N.M.G. and Kossen N.W.F. (1984) Dissolved-oxygen concentration profiles in a production-scale bioreactor. Biotechnol. Bioeng. 26: 546-550.
2. Larsson G. and Enfors S.O. (1985) Influence of oxygen starvation on the respiratory capacity of Penicillium chrysogenum. Appl. Microbiol. Biotechnol. 21: 228-233.
3. Enfors S.O., Jahic M., Rozkov A., et al. (2001) Physiological responses to mixing in large scale bioreactors. Journal Biotechnol. 85: 175- 185.